【調査レポート】機能性表示食品制度と米国ダイエタリーサプリメント制度の比較~「健康被害情報の報告体制」「製造・品質管理体制」を中心に~
健康食品業界に特化したコンサルティング会社である株式会社グローバルニュートリショングループ(本社:東京都豊島区西池袋5-17-11、代表取締役:武田 猛)は、紅麹問題で混乱している社会、不安を感じている消費者に対して客観的な判断に役立ててもらうために、機能性表示食品制度と米国ダイエタリーサプリメント制度を比較、分析を行いました。その結果、機能性表示食品制度は高い透明性を持つが、「新規原料」「GMP」「有害事象の報告」は米国ダイエタリーサプリメント制度が先行していることが明らかになりました。
調査の背景
紅麹問題で混乱している社会、不安を感じている消費者に対して客観的な判断に役立ててもらうために、これまで蓄積した知見を基に「機能性表示食品制度自体の問題」と、「食品全般にかかわる問題」を分けて整理・分析を実施しました。最初に、「健康食品の健康被害情報の収集・報告体制の在り方」「製造・品質管理の在り方(GMPを含む)」について、機能性表示食品制度設計時の参考とされた米国ダイエタリーサプリメント制度(ダイエタリーサプリメント健康教育法:DSHEA)と機能性表示食品制度を比較するとともに、米国ダイエタリーサプリメント市場の歴史を俯瞰し、ポイントを整理しました。
機能性表示食品制度と米国ダイエタリーサプリメント制度との比較、分析の主な結果
■機能性表示食品制度は透明性が高いことが判明
機能性表示食品制度は、安全性の根拠、機能性の根拠、品質管理体制等を消費者庁に販売前に届出をし、その内容が消費者庁のHP上で公表されます。一方、ダイエタリーサプリメント制度では、機能性表示の内容と成分を販売後30日以内にFDAに届出をする制度です。機能性の根拠は届出する必要はありません。
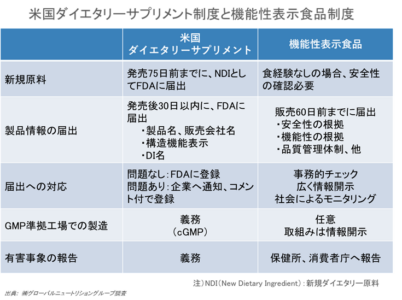
機能性表示食品制度は米国の制度と比べて透明性が高いことから、その分、疑義が出やすく、届出撤回の件数も多数に上ると考察されます。
■「GMP」「有害事象の報告」は米国ダイエタリーサプリメント制度が先行
一方、「新規原料」の扱い、「GMP(Good Manufacturing Practice:適正製造規範)」の義務化、「有害事象の報告」義務は、米国ダイエタリーサプリメント制度の方が先行しています。米国ダイエタリーサプリメント制度を巡る歴史を振り返ってみます(別添「米国ダイエタリーサプリメント関連法規の変遷」をご参照ください)。米国ダイエタリーサプリメント制度は、施行当初は品質問題や健康被害、機能性の科学的根拠のあり方等に問題が山積しましたが、一つ一つ法律やガイダンスで対応し、今日に至っています。今年は制度施行30周年です。
■「有害事象の報告」は期日を設定。しかし、風評被害にも配慮。
「ダイエタリーサプリメントおよび非処方箋薬に対する消費者保護法(Dietary Supplement and Nonprescription Drug Consumer Protection Act)」では、有害事象(Adverse Event)をダイエタリーサプリメントの使用によって生じる健康に係る事象で有害(不都合)なもの、と定義しています。そして、事業者は、入手した重篤な有害事象に関する報告を15営業日以内にFDA長官に届けなければならない、とされています。但し、「保護されるべき情報」として、重篤な有害事象に関する報告、更新情報、及びそれ以外で、FDA長官に自発的に提出された有害事象報告は、有害事象について公表された安全性情報が、当該製品と有害事象との因果関係を認めるものではないこと、と示されています。また、「解釈のルール」として、総ての有害事象報告はその提出をもって、当該ダイエタリーサプリメントが当該有害事象の原因になっていると認めるような解釈はしてはならないとされており、事業者が有害事象の届出を躊躇することがないように配慮もされています。
これに対し、機能性表示食品制度では、健康被害情報の収集・報告について「健康被害の発生及び拡大のおそれがある場合は、消費者庁食品表示課へ速やかに報告する。」「健康被害情報に係る都道府県等(保健所)に対する報告については、食品衛生法等の関係規定に従い適切に行う。」とガイドラインに示されています。
■厳格な米国GMP
米国ダイエタリーサプリメントは、GMP準拠が義務付けられていますが、機能性表示食品は「サプリメント形状の加工食品については、GMPに基づく製造工程管理が強く望まれる」とガイドラインに示されています。そしてそのGMPの内容も、日米では違いがあります。
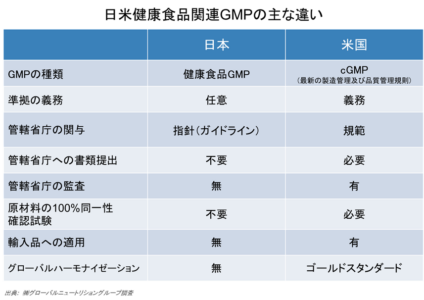
最も大きな違いは、米国は国(FDA)がGMP規範を作り、監査(査察)を行っていますが、日本は国が指針を示すにとどまり、規範は業界団体等民間に任せていて、その監査も民間が実施しています。そしてもう1点、原材料の100%同一性確認試験を義務付けている点が、米国GMPが厳格と言われる理由でもあります。
■今回の調査を通じて
機能性表示食品制度は米国ダイエタリーサプリメント制度を参考に策定されました。その際、米国制度の良い点や欠点を調査しました。しかし、健康被害情報の報告の義務化や健康食品GMPの義務化などは厚生労働省の所管となり、食品全般に関する食品安全行政には手つかずの状況の中で、機能性表示食品制度がスタートした経緯があります。その結果、透明性が高いという長所を持ちながらも、安全性、品質管理体制、健康被害情報の報告について不十分な点が残ったということが、今回の比較・分析から明らかになりました。
調査の詳細
株式会社グローバルニュートリショングループが過去に調査した、米国ダイエタリーサプリメント制度を再度確認し、機能性表示食品制度ガイドライン、消費者庁が実施した検証事業の報告書等の内容と比較しました。
株式会社グローバルニュートリショングループ について
株式会社グローバルニュートリショングループは、グローバルなネットワークを有する、健康食品業界に特化したコンサルティングファームです。現在まで、海外20か国とのビジネスを経験し、国内外合わせて750件以上のプロジェクトを実施してきました。
世界各地にネットワークを築き上げ、情報活用サービス「グローバルニュートリション研究会」を設立、コンサルティング業務として食品会社、化粧品会社、製薬会社の健康食品部門に対して、商品開発、マーケティング、海外進出などのコンサルティングを行っています。
「世界全体の中で日本を位置付け、自らのビジネスを正確に位置付ける」という「グローバルセンス」のもとに先行する欧米トレンドを取り入れたコンセプトメイキングを得意としています
【会社概要】
社 名: 株式会社グローバルニュートリショングループ
本社所在地: 東京都豊島区西池袋 5-17-11
代表者取締役:武田 猛
創立:2004年1月5日
HP: https://global-nutrition.co.jp/
事業内容:
・健康食品(サプリメント、機能性食品)に関するコンサルティング業務
・健康食品(サプリメント、機能性食品)の市場調査・分析
・健康食品(サプリメント、機能性食品)の新商品開発、マーケティング支援
・機能性表示食品届出サポート
・海外企業の日本市場参入の支援
・日本企業の海外市場進出の支援
【報道機関からの問い合わせ先】
TEL:03-5944-9813 広報担当:鈴木、有松
e-mail:info@global-nutrition.co.jp
◎本プレスリリースのPDFファイルはこちら

